Открытие метода вакцинации дало старт новой эре борьбы с болезнями.
В состав прививочного материала входят убитые или сильно ослабленные микроорганизмы либо их компоненты (части). Они служат своеобразным муляжом, обучающим иммунную систему давать правильный ответ инфекционным атакам. Вещества, входящие в состав вакцины (прививки), не способны вызвать полноценное заболевание, но могут дать возможность иммунитету запомнить характерные признаки микробов и при встрече с настоящим возбудителем быстро его определить и уничтожить.
Производство вакцин получило массовые масштабы в начале ХХ века, после того как фармацевты научились обезвреживать токсины бактерий. Процесс ослабления потенциальных возбудителей инфекций получил название аттенуации.
Сегодня медицина располагает более, чем 100 видами вакцин от десятков инфекций.
Препараты для иммунизации по основным характеристикам делятся на три основных класса.
- Живые вакцины. Защищают от полиомиелита, кори, краснухи, гриппа, эпидемического паротита, ветряной оспы, туберкулеза, ротавирусной инфекции. Основу препарата составляют ослабленные микроорганизмы - возбудители болезней. Их сил недостаточно для развития значительного недомогания у пациента, но хватает, чтобы выработать адекватный иммунный ответ.
- Инактивированные вакцины. Прививки против гриппа, брюшного тифа, клещевого энцефалита, бешенства, гепатита А, менингококковой инфекции и др. В составе мертвые (убитые) бактерии или их фрагменты.
- Анатоксины (токсоиды). Особым образом обработанные токсины бактерий. На их основе делают прививочный материал от коклюша, столбняка, дифтерии.
В последние годы появился еще один вид вакцин - молекулярные. Материалом для них становятся рекомбинантные белки или их фрагменты, синтезированные в лабораториях путем применения методов генной инженерии (рекомбининтная вакцина против вирусного гепатита В).
Схемы изготовления некоторых видов вакцин
Живые бактериальные
Схема подходит для вакцины БЦЖ, БЦЖ-М.
Живые противовирусные

Схема подходит для производства вакцин от гриппа, ротавируса, герпеса I и II степеней, краснухи, ветряной оспы.
Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться:
- куриные эмбрионы;
- перепелиные эмбриональные фибробласты;
- первичные клеточные культуры (куриные эмбриональные фибробласты, клетки почек сирийских хомячков);
- перевиваемые клеточные культуры (MDCK, Vero, MRC-5, BHK, 293).
Первичный сырьевой материал очищают от клеточного дебриса в центрифугах и с помощью сложных фильтров.
Инактивированные антибактериальные вакцины
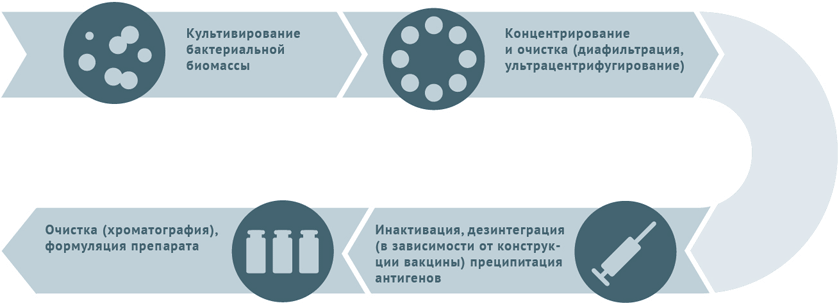
- Культивация и очистка штаммов бактерий.
- Инактивация биомассы.
- Для расщепленных вакцин клетки микробов дезинтегрируют и осаждают антигены с последующим их хроматографическим выделением.
- Для конъюгированных вакцин полученные при предыдущей обработке антигены (как правило, полисахаридные) сближают с белком-носителем (конъюгация).
Инактивированные противовирусные вакцины

- Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться куриные эмбрионы, перепелиные эмбриональные фибробласты, первичные клеточные культуры (куриные эмбриональные фибробласты, клетки почек сирийских хомячков), перевиваемые клеточные культуры (MDCK, Vero, MRC-5, BHK, 293). Первичная очистка для удаления клеточного дебриса проводится методами ультрацентрифугирования и диафильтрации.
- Для инактивации используются ультрафиолет, формалин, бета-пропиолактон.
- В случае приготовления расщепленных или субъединичных вакцин полупродукт подвергают действию детергента с целью разрушить вирусные частицы, а затем выделяют специфические антигены тонкой хроматографией.
- Человеческий сывороточный альбумин применяется для стабилизации полученного вещества.
- Криопротекторы (в лиофилизатах): сахароза, поливинилпирролидон, желатин.
Схема подходит для производства прививочного материала против гепатита А, желтой лихорадки, бешенства, гриппа, полиомиелита, клещевого и японского энцефалитов.
Анатоксины

Для дезактивации вредного воздействия токсинов используют методы:
- химический (обработка спиртом, ацетоном или формальдегидом);
- физический (подогрев).
Схема подходит для производства вакцин против столбняка и дифтерии.
По данным Всемирной Организации Здравоохранения (ВОЗ), на долю инфекционных заболеваний приходится 25 % от общего количества смертей на планете ежегодно. То есть инфекции до сих пор остаются в списке главных причин, обрывающих жизнь человека.
Одним из факторов, способствующих распространению инфекционных и вирусных заболеваний, являются миграция потоков населения и туризм. Перемещение человеческих масс по планете влияет на уровень здоровья нации даже в таких высокоразвитых странах, как США, ОАЭ и государства Евросоюза.
По материалам: «Наука и жизнь» № 3, 2006, «Вакцины: от Дженнера и Пастера до наших дней», академик РАМН В. В. Зверев, директор НИИ вакцин и сывороток им. И. И. Мечникова РАМН.
Задать вопрос специалисту
Вопрос экспертам вакцинопрофилактики
Вопросы и ответы
Вакцина "Менюгейт" зарегистрирована в России? С какого возраста разрешена к применению?
Да, зарегистрирована, вакцина – от менингококка С, сейчас также есть вакцина конъюгированная, но уже против 4 типов менингококков – А, С, Y, W135 – Менактра. Прививки проводят с 9 мес.жизни.
Муж транспортировал вакцину РотаТек в другой город.Покупая ее в аптеке мужу посоветовали купить охлаждающий контейнер,и перед поездкой его заморозить в морозильной камере,потом привязать вакцину и так ее транспортировать. Время в пути заняло 5 часов. Можно ли вводить такую вакцину ребенку? Мне кажется,что если привязать вакцину к замороженному контейнеру, то вакцина замерзнет!
Отвечает Харит Сусанна Михайловна
Вы абсолютно правы, если в контейнере был лед. Но если там была смесь воды и льда- вакцина не должна замерзать. Однако живые вакцины, к которым относится ротавирусная, не увеличивают реактогенность при температуре менее 0, в отличие от неживых, а, например, для живой полиомиелитной допускается замораживание до -20 град С.
Моему сыну сейчас 7 месяцев.
В 3 месяца у него случился отек Квинке на молочную смесь Малютка.
Прививку от гепатита сделали в роддоме, вторую в два месяца и третью вчера в семь месяцев. Реакция нормальная, даже без температуры.
Но вот на прививку АКДС нам устно дали медотвод.
Я за прививки!! И хочу сделать прививку АКДС. Но хочу сделать ИНФАНРИКС ГЕКСА. Живем в Крыму!!! В крыму ее нигде нет. Посоветуйте как поступить в такой ситуации. Может есть зарубежный аналог? Бесплатную делать категорически не хочу. Хочу качественную очищеную, что бы как монжно меньше риска!!!
В Инфанрикс Гекса содержится компонент против гепатита В. Ребенок полностью привит против гепатита. Поэтому в качестве зарубежного аналога АКДС можно сделать вакцину Пентаксим. Кроме того, следует сказать, что отек Квинке на молочную смесь не является противопоказанием к вакцине АКДС.
Подскажите, пожалуйста, на ком и как тестируют вакцины?
Отвечает Полибин Роман Владимирович
Как и все лекарственные препараты вакцины проходят доклинические исследования (в лаборатории, на животных), а затем клинические на добровольцах (на взрослых, а далее на подростках, детях с разрешения и согласия их родителей). Прежде чем разрешить применение в национальном календаре прививок исследования проводят на большом числе добровольцев, например вакцина против ротавирусной инфекции испытывалась почти на 70 000 в разных странах мира.
Почему на сайте не представлен состав вакцин? Почему до сих пор проводится ежегодная реакция Манту (зачастую не информативна), а не делается анализ по крови, например, квантифероновый тест? Как можно утверждать реакции иммунитета на введенную вакцину, если еще ни кому не известно в принципе, что такое иммунитет и как он работает, особенно если рассматривать каждого отдельно взятого человека?
Отвечает Полибин Роман Владимирович
Состав вакцин изложен в инструкциях к препаратам.
Реакция Манту. По Приказу № 109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерациии» и Санитарным правилам СП 3.1.2.3114-13 "Профилактика туберкулеза", несмотря на наличие новых тестов, детям необходимо ежегодно делать реакцию Манту, но так как этот тест может давать ложноположительные результаты, то при подозрении на тубинфицирование и активную туберкулезную инфекцию проводят Диаскин-тест. Диаскин-тест является высоко чувствительным (эффективным) для выявления активной туберкулезной инфекции (когда идет размножение микобактерий). Однако полностью перейти на Диаскин-тест и не делать реакцию Манту фтизиатры не рекомендуют, так как, он не "улавливает" раннее инфицирование, а это важно, особенно для детей, поскольку профилактика развития локальных форм туберкулеза эффективна именно в раннем периоде инфицирования. Кроме того, инфицирование микобактерией туберкулеза необходимо определять для решения вопроса о ревакцинации БЦЖ. К сожалению, нет ни одного теста, который бы со 100% точностью ответил на вопрос, есть инфицирование микобактерией или заболевание. Квантифероновый тест также выявляет только активные формы туберкулеза. Поэтому при подозрении на инфицирование или заболевание (положительная реакция Манту, контакт с больным, наличие жалоб и пр.) используются комплексные методы (диаскин-тест, квантифероновый тест, рентгенография и др.).
Что касается «иммунитета и как он работает», в настоящее время иммунология - это высокоразвитая наука и многое, в частности, что касается процессов на фоне вакцинации – открыто и хорошо изучено.
Ребёнку 1 год и 8 месяцев, все прививки ставились в соответствии с календарем прививок. В том числе 3 пентаксима и ревакцинация в полтора года тоже пентаксим. В 20 месяцев надо ставить от полиомиелита. Очень всегда переживаю и отношусь тщательно к выбору нужных прививок, вот и сейчас перерыла весь интернет, но так и не могу решить. Мы ставили всегда инъекцию (в пентаксиме). А теперь говорят капли. Но капли-живая вакцина, я боюсь различных побочек и считаю, что лучше перестраховаться. Но вот читала, что капли от полиомиелита вырабатывают больше антител, в том числе и в желудке, то есть более эффективные, чем инъекция. Я запуталась. Поясните, инъекция менее эффективна (имовакс-полио, например)? Отчего ведутся такие разговоры? У каплей боюсь хоть и минимальный, но риск осложнения в виде болезни.
Отвечает Полибин Роман Владимирович
В настоящее время Национальный календарь прививок России предполагает комбинированную схему вакцинации против полиомиелита, т.е. только 2 первых введения инактивированной вакциной и остальные – оральной полиовакциной. Это связано с тем, чтобы полностью исключить риск развития вакциноассоциированного полиомиелита, который возможен только на первое и в минимальном проценте случаев на второе введение. Соответственно, при наличии 2-х и более прививок от полиомиелита инактивированной вакциной, осложнения на живую полиовакцину исключены. Действительно, считалось и признается некоторыми специалистами, что оральная вакцина имеет преимущества, так как формирует местный иммунитет на слизистых кишечника в отличие от ИПВ. Однако сейчас стало известно, что инактивированная вакцина в меньшей степени, но также формирует местный иммунитет. Кроме того, 5 введений вакцины против полиомиелита как оральной живой, так и инактивированной вне зависимости от уровня местного иммунитета на слизистых оболочках кишечника, полностью защищают ребенка от паралитических форм полиомиелита. В связи с вышесказанным вашему ребенку необходимо сделать пятую прививку ОПВ или ИПВ.
Следует также сказать, что на сегодняшний день идет реализация глобального плана Всемирной организации здравоохранения по ликвидации полиомиелита в мире, которая предполагает полный переход всех стран к 2019 году на инактивированную вакцину.
В нашей стране уже очень долгая история использования многих вакцин – ведутся ли долгосрочные исследования их безопасности и можно ли ознакомиться с результатами воздействия вакцин на поколения людей?
Отвечает Шамшева Ольга Васильевна
За прошлый век продолжительность жизни людей возросла на 30 лет, из них 25 дополнительных лет жизни люди получили за счет вакцинации. Больше людей выживают, они живут дольше и качественнее за счет того, что снизилось инвалидность из-за инфекционных заболеваний. Это общий ответ на то, как влияют вакцины на поколения людей.
На сайте Всемирной Организации Здравоохранения (ВОЗ) есть обширный фактический материал о благотворном влиянии вакцинации на здоровье отдельных людей и человечества в целом. Отмечу, что вакцинация –это не система верований, это - область деятельности, опирающаяся на систему научных фактов и данных.
На основании чего мы можем судить о безопасности вакцинации? Во-первых, ведется учет и регистрация побочных действий и нежелательных явлений и выяснение их причинно-следственной связи с применением вакцин (фармаконадзор). Во-вторых, важную роль в отслеживании нежелательных реакций играют постмаркетинговые исследования (возможного отсроченного неблагоприятного действия вакцин на организм), которые проводят компании - владельцы регистрационных свидетельств. И, наконец, проводится оценка эпидемиологической, клинической и социально-экономической эффективности вакцинации в ходе эпидемиологических исследований.
Что качается фармаконадзора, то у нас в России система фармаконадзора только формируется, но демонстрирует очень высокие темпы развития. Только за 5 лет число зарегистрированных сообщений о нежелательных реакциях на лекарственные средства в подсистему «Фармаконадзор» АИС Росздравнадзора выросло в 159 раз. 17 033 жалобы в 2013 году против 107 в 2008. Для сравнения – в США в год обрабатываются данные около 1 млн случаев. Система фармаконадзора позволяет отслеживать безопасность препаратов, накапливаются статистические данные, на основании которых может измениться инструкция по медицинскому применению препарата, препарат может быть отозван с рынка и т.п. Таким образом, обеспечивается безопасность пациентов.
И по закону «Об обращении лекарственных средств» от 2010 года врачи обязаны сообщать федеральным органам контроля обо всех случаях побочного действия лекарственных средств.
В мире существует столько лекарств, что, казалось бы, с ними можно вылечить любую болезнь. Фармацевтические компании постоянно выпускают новые препараты. Действительно, в своё время открытие пенициллина перевернуло мир. Сейчас человек шагнул ещё дальше. Однако некоторые болезни вылечить нельзя, единственная возможность защититься от них – вакцинация.
В мире официально применяется несколько сотен разновидностей вакцинных препаратов. Сюда включены не только инактивированные, рекомбинантные, химические, но и живые, формирующие иммунитет против ряда инфекционных заболеваний (бешенства, дифтерии, коклюша, кори, краснухи, полиомиелита, столбняка и других). А ещё чуть более века назад в медицинской практике использовалось только пять вакцин. Это были живые против бешенства, натуральной оспы и чумы, и инактивированные – от брюшного тифа и холеры. Такой ограниченный инструментарий объяснялся тем, что исследования заболеваний, чья этиология была предположительно инфекционной, производились на некрупных животных в лабораториях, которые были невосприимчивы к человеческим патогенам.
Революционное открытие было сделано в 1954 году американскими учёными Эндерсом, Уэллером и Роббинсом (за которое впоследствии они были удостоены Нобелевской премии). Они доказали на примере вируса полиомиелита, что патогенные микроорганизмы можно выращивать в культурах различных тканей. Это «развязало руки» иммунологам и вирусологам, предоставило им широкие возможности для изучения этиологической роли разных возбудителей, получения образцов штаммов с целью последующего использования их для прививок. Примерно тогда же стало понятно, что некоторые виды приматов чувствительны к инфекционным агентам, которые ранее считались опасными только для человека. Это позволило проводить лабораторные эксперименты на обезьянах.
Сегодняшние прививочные средства имеют различные варианты состава. Фармацевты делают все, чтобы прививка переносилась легче. Всё же самыми эффективными были и остаются живые вакцины. В них входят живые микроорганизмы, отсюда и название. О формах, свойствах и безопасности таких препаратов – в статье.
Живая вакцина – препарат, который используют для иммунизации. В его составе – обезвреженные штаммы микроорганизмов, вызывающих болезнь, они начинают распространяться в месте укола. Заболевание не прогрессирует, однако иммунитет формируется, причём стойкий – гуморальный, клеточный и секреторный.
Ослабленные штаммы получают в процессе деактивации гена, отвечающего за заразность бактерии. Обезвреживания добиваются различными способами – химическими или физическими (например, воздействием высоких температур). Обычно живые вакцины представляют собой порошок, который растворяют в жидкости для инъекции. Сухие препараты хранятся дольше и не повреждаются при транспортировке. Однократное введение средства способствует выработке иммунитета.

Одним из видов живых вакцин являются дивергентные. Они изготавливаются из микроорганизмов, находящихся в близком родстве с возбудителем инфекции, но вызвать заболевание не могут. Самый яркий пример подобного препарата – БЦЖ, в основе средства – бактерии не человеческого, а бычьего туберкулёза.
Чем отличается живая вакцина от неживой
Основная разница между живой и неживой вакцинами – то, что в основе первой содержатся живые микроорганизмы. Многие полагают, что поэтому она лучше и безопаснее, поскольку более естественна. На самом деле, это не совсем так. В различиях следует разобраться подробнее.
- Безопасность в применении. По этому поводу было проведено много исследований, в результате которых выявлено, что ни одно из средств не может спровоцировать аллергию. Уровень безопасности одинаковый. При этом живые вакцины всё же не применяют у пациентов с такими болезнями, как ВИЧ или онкология, чтобы не ослабить иммунитет ещё больше, ведь при введении живого микроба, пусть и инактивированного, есть вероятность развития настоящего заболевания.
- Достижение эффекта. Живая вакцина при однократном введении способна сформировать иммунитет на длительный срок. Неживая требует ревакцинации, хотя эффект тоже достаточно хорош.
- Воздействие. Действующие вещества живых препаратов начинают работу мгновенно, результат появляется сразу. Чтобы добиться эффекта от неживой вакцины, нужно завершить курс, включающий обычно два или три укола.
Существенных различий между живыми и неживыми вакцинами нет, поэтому, изучив инструкции к ним, пациент сам принимает решение о необходимости использования того или иного препарата.
Виды и их характеристика
Сегодня в медицине используются следующие виды вакцин.
- Живые. В их составе – живые микроорганизмы, провоцирующие развитие заболевания. Однако они были очищены в лаборатории. Такие прививки особенно тяжело переносятся организмом, так как оказывают на иммунную систему сильное давление. Иммунитет, создаваемый подобными препаратами, похож на естественный, выработанный после перенесённой болезни. Поэтому считается, что данные вакцинные составы наиболее эффективны.
- Химические. В состав таких препаратов входят антигены бактерий, полученные химическими способами. Попадая в организм, они мгновенно рассасываются, иммунная система не распознаёт их как «врагов». Обычно их используют в сочетании с другими вакцинами для формирования иммунитета против нескольких вирусов сразу.
- Корпускулярные. Этот вид вакцин содержит в формуле убитые клетки микробов, следовательно, воздействие на организм минимально. Однако иммунная система распознаёт чужеродное тело и начинает с ним бороться. Срок действия у такого препарата короче, чем у живого аналога, поэтому требуется ревакцинация.
- Анатоксины. Есть такие микроорганизмы, которые выделяют опасные вещества при попадании в организм. Именно эти токсины виноваты в развитии симптомов болезни. Анатоксины изготавливают из них, очищая при помощи формалина. Иммунитет после их введения менее стойкий, чем естественный, приобретённый после заболевания. Попытки улучшить данный вид вакцин продолжаются.
- Рекомбинантные. Новый тип действующего вещества в вакцинном препарате. Его получают посредством клонирования генов микробных частиц, затем созданные гены вводят в грибки или бактерии, получают клетки, из которых выделяют новые частицы. Плюсы подобных вакцин – эффективность и безопасность.
- Инактивированные. Их также можно назвать убитыми. Есть ещё название «мертвая» вакцина, поскольку микроорганизм, вызывающий болезнь, умерщвляют. На вирус или бактерию воздействуют, например, посредством температуры, и они погибают. Такие препараты отличаются безопасностью и стабильностью. Прививать ними можно, не опасаясь, что вирус распространится и проявит свои симптомы. Однако иммунный ответ будет слабее. В инактивированной вакцине «убитым» бывает либо целый микроорганизм, либо его составляющая часть.
Какие вакцины относятся к живым: полный перечень
Эпидемические вспышки брюшного тифа, кори, краснухи, полиомиелита, эпидемического паротита, зафиксированные в странах Европы и Северной Америки во второй половине 20-го столетия, определили вектор медицинских исследований в то время. В результате таких изысканий, уже к началу 70-х годов врачи оперировали тремя десятками живых вакцин.
Не во всех случаях применяют живые вакцины. Однако перечень болезней, от которых ними прививают, широк и включает такие инфекции, как:
- полиомиелит;
- туберкулёз;
- паротит;
- оспа;
- корь;
- бешенство;
- грипп;
- туляремия;
- сибирская язва;
- чума;
- краснуха;
- некоторые виды лихорадок.
В списке – обязательные прививки, предусмотренные календарём, и те, которые ставят по желанию.
Технология получения
Получение живых вакцин – процесс, включающий в себя множество этапов.
Бактериальные вакцины получают по такому алгоритму.
- Выращивание бактерий в питательной среде.
- Концентрирование и очищение.
- Формуляция и высушивание.

Противовирусные препараты синтезируют следующим образом.
- Выращивание штамма на клетках или эмбрионе курицы.
- Очистка и концентрирование.
- Высушивание.
Механизм, как правило, похож. Отличается он в случае производства ослабленных вакцин. Около девяти лет уходит на создание такого препарата, поскольку требуется многократно синтезировать и очищать полученные клетки.
Особенности применения
При использовании живых вакцин следует строго соблюдать правила хранения и интервал между инъекциями. Минимальный промежуток – 1 месяц, иначе высок риск появления побочных эффектов.
Нельзя замораживать препарат, а также перевозить его во вскрытой упаковке.
Прививку делают подкожно или накожно. Важно, чтобы средство не распространилось по всему телу, иначе осложнений не избежать.
Есть препараты, применяемые перорально, например, вакцина от полиомиелита. После её введения нельзя есть и употреблять жидкости несколько часов.
Вакцину от гриппа применяют интраназально.
Когда вскрывается ампула, важно избегать перепадов температур.
Иммунизация живыми вакцинами осуществляется не всегда. Существует ряд противопоказаний. Так, нельзя применять живые вакцины у:
- беременных женщин – это может отрицательно повлиять на будущего малыша;
- лиц, страдающих лейкозом или лейкомой;
- пациентов, лечащихся иммунодепрессантами, стероидами, иначе эффект от терапии будет потерян;
- детей с иммунодефицитом;
- лиц, которые на момент прививки болеют, – следует дождаться выздоровления, в противном случае от вакцинации пользы ожидать не стоит.

Механизм действия
Живая вакцина включает в себя обезвреженные микроорганизмы. Они прошли этап очищения, поэтому не способны вызвать болезнь. А вот спровоцировать иммунную систему на ответ и формирование реакции они могут без труда.
Проникая в организм, ослабленные микробы пытаются ему навредить, тут и запускается защитный процесс – вырабатываются антитела к инфекции.
Так формируется стойкий защитный барьер против введённого возбудителя болезни.
Безопасность подобных препаратов доказана клинически, тем не менее, некоторые врачи продолжают сомневаться, особенно когда речь идёт об иммунизации детей.
Несмотря на это мнение, дети прививаются успешно, получая крепкий иммунитет благодаря живым вакцинам.
Как характеризуется иммунный ответ
После того, как живые бактерии препарата вводятся в организм, включается защитная функция – начинают вырабатываться антитела. В случае с живой вакциной этот процесс запускается практически мгновенно, то есть сразу после попадания состава под кожу. По статистике, скорость формирования иммунного ответа в два раза превышает скорость ответа после введения неживой вакцины. Поэтому, как правило, повторное введение не требуется или происходит через длительное время.
Иногда наблюдаются такие проявления, как гипертермия, слабость или сонливость. Некоторые пациенты теряют аппетит и жалуются на быструю утомляемость. Все эти реакции считаются нормальными и означают, что иммунная система борется с «незваным гостем».
Об эффективности иммунного ответа судят по количеству выработанных антител. Проверить этот показатель можно спустя неделю, тогда результат будет наиболее информативен.
На выработку антител также влияет ряд факторов, зависящих от вакцины и от организма.
К первым относятся:
- чистота вещества;
- время жизни антигена;
- доза;
- наличие защитных антигенов;
- частота введения.

Факторы со стороны организма:
- индивидуальная иммунная реактивность;
- возраст;
- нормальность или ослабленность иммунитета;
- общее состояние;
- генетические особенности.
Можно также выделить факторы внешней среды:
- особенности питания;
- условия жизни и работы;
- климатические условия.
В целом, эффективность вакцины оценивается по следующим критериям.
- Безопасность. Важно, чтобы препарат не вызывал смертельных исходов.
- Защита. Вакцина должна формировать иммунитет против вируса, штамм которого она включает.
- Поддержание защитного иммунитета. Эффект должен сохраняться как можно дольше.
- Индукция нейтрализующих компонентов. Нейтрализующие антитела нужны, чтобы избежать заражения.
- Индукция защитных Т-клеток. Именно этот вид клеток наиболее эффективно контролирует распространение вредных микроорганизмов.
- Практические соображения. Удобство и длительность хранения, простота использования и стоимость.
Основные достоинства
В медицинской среде до сих пор ведутся споры о безопасности применения живых вакцин. Несмотря на это, большинство всё же считает, что у таких препаратов достоинства превышают недостатки. К положительным сторонам живых вакцин относятся:
- возможность вводить препарат один раз в минимальной дозе, что никак не влияет на эффективность;
- длительность и прочность иммунного ответа;
- различные варианты введения (подкожно, накожно, перорально, интраназально);
- быстрая реакция иммунной системы;
- относительно простое изготовление;
- длительное хранение при соблюдении всех условий;
- небольшая цена.

Существенные недостатки
Однако и без недостатков не обошлось. Как и другие препараты, живая вакцина имеет свои минусы:
- если прививку делать на фоне ослабленного иммунитета, возможно, появятся осложнения;
- ослабленные антигены получают достаточно долго (ранее говорилось, что иногда может понадобиться около девяти лет на выведение определённого штамма);
- из-за неправильного хранения или перевозки вакцина может испортиться;
- сложно рассчитать дозу, во многих случаях её должен индивидуально подбирать врач;
- есть вероятность занесения в организм латентных вирусов, поскольку в препарате содержатся их клетки (особенно это опасно при онкологии).
Длительный опыт вакцинопрофилактики (в Российской Федерации и за рубежом) свидетельствует о том, что риск возникновения постпрививочных осложнений и их тяжесть несоизмеримо ниже опасности развития последствий заражения инфекциями, от которых эти прививки защищают.
К вопросу вакцинации надо подходить очень серьёзно, особенно когда она касается детей. Выбор правильного препарата способен укрепить здоровье, а в некоторых случаях даже спасти жизнь, если начинается эпидемия того или иного заболевания. Перед проведением процедуры необходимо прочитать инструкцию по применению препарата, изучить противопоказания. Родителям важно помнить, что перед прививкой ребёнка должен осмотреть специалист, назначить анализы, чтобы убедиться, что в организме нет воспалительных процессов.
Разумный подход к иммунизации защитит от опасных болезней на долгий срок. Несмотря на то, что в медицинской практике уже активно используются вакцинные средства третьего и четвёртого поколений, живые аттенуированные вакцины по-прежнему актуальны. Они до сих пор считаются эффективными иммунобиологическими препаратами.
Живые вирусные вакцины - это, как правило, искусственно ослабленные посредством культивирования или природные авирулентные либо слабовирулентные иммуногенные штаммы вируса, которые, размножаясь в естественно восприимчивом организме, не проявляют повышения вирулентности и потеряли способность к горизонтальной передаче.
Безопасные высокоиммуногенные живые вакцины являются лучшими из всех существующих вирусных вакцин. Применение многих из них дало блестящие результаты в борьбе с наиболее опасными вирусными болезнями человека и животных. В основе эффективности живых вакцин лежит имитация субклинической инфекции. Живые вакцины вызывают иммунный ответ на каждый протективный антиген вируса.
Основным преимуществом живых вакцин считается активизация всех звеньев иммунной системы, вызывающая сбалансированный иммунный ответ (системный и локальный, иммуноглобулиновый и клеточный). Это имеет особое значение при тех инфекциях, когда клеточный иммунитет играет важную роль, а также при инфекциях слизистых оболочек, где требуется как системный, так и локальный иммунитет. Местное применение живых вакцин обычно является более эффективным для стимулирования локального ответа у непраймированных хозяев, чем инактивированные вакцины, вводимые парентерально.
В идеале, вакцинация должна повторять иммунологические стимулы естественной инфекции , сводя до минимума нежелательные эффекты. Она должна вызывать напряженный продолжительный иммунитет при введении в небольшой дозе. Ее введение, как правило, не должно сопровождаться слабой, кратковременной общей и местной реакцией. Хотя после введения живой вакцины иногда допускается развитие у небольшой части реципиентов отдельных слабовыраженных клинических признаков, напоминающих легкое течение естественной болезни. Живые вакцины больше, чем другие, отвечают этим требованиям и, кроме того, отличаются низкой стоимостью и простотой применения разными способами.
Вакцинные вирусные штаммы
должны обладать генетической и фенотипической стабильностью. Их приживляемость в привитом организме должна быть выраженной, а способность к размножению ограниченной. Вакцинные штаммы обладают значительно менее выраженной инвазивностью, чем их вирулентные предшественники. Это связано в значительной мере с их частично ограниченной репликацией в месте проникновения и в органах-мишенях естественного хозяина. Репликация вакцинных штаммов в организме легче ограничивается естественными неспецифическими защитными механизмами. Вакцинные штаммы размножаются в привитом организме до тех пор, пока его защитные механизмы не затормозят их развитие.
В течение этого времени образуется такое количество антигена
, которое значительно превышает его при введении с инактивированной вакциной.
Для аттенуации вирусов обычно применяют пассажи вируса в неестественном хозяине или культуре клеток, пассажи при пониженной температуре и мутагенез с последующей селекцией мутантов с измененным фенотипом.
Большинство современных живых вакцин , используемых для профилактики инфекционных болезней человека и животных, получены пассажами вирулентного вируса в гетерологичном хозяине (животные, куриные эмбрионы, различные клеточные культуры). Аттенуированные в чужеродном организме вирусы приобретают множественные мутации в геноме, препятствующие реверсии вирулентных свойств.
В настоящее время в практике широко применяют живые вакцины против многих вирусных заболеваний человека (полиомиелит, желтая лихорадка, грипп, корь, краснуха, паротит и др.) и животных (чума крупного рогатого скота, свиней, плотоядных, бешенство, герпес-, пикорна-, коронавирусные и другие болезни). Однако еще не удалось получить эффективных вакцин против ряда вирусных болезней человека (СПИД, парагрипп, респираторно-синциальная инфекция, денгевирусная инфекция и другие) и животных (африканская чума свиней, инфекционная анемия лошадей и другие).
Имеется много примеров тому, что традиционные методы аттенуации вирусов еще не исчерпали своих возможностей и продолжают играть существенную роль в разработке живых вакцин. Однако их значение постепенно уменьшается по мере увеличения масштабов использования новой технологии конструирования вакцинных штаммов. Несмотря на значительный прогресс в этой области, принципы получения живых вирусных вакцин, заложенные Л. Пастером, до сих пор не потеряли своей актуальности.
Они содержат ослабленный живой микроорганизм. Примером могут служить вакцины против полиомиелита, кори, паротита, краснухи или туберкулеза. Могут быть получены путем селекции (БЦЖ, гриппозная). Они способны размножаться в организме и вызывать вакцинальный процесс, формируя невосприимчивость. Утрата вирулентности у таких штаммов закреплена генетически, однако у лиц с иммунодефицитами могут возникнуть серьезные проблемы. Как правило, живые вакцины являются корпускулярными. Живые вакцины получают путем искусственного аттенуирования (ослабления штамма (BCG - 200-300 пассажей на желчном бульоне, ЖВС - пассаж на ткани почек зеленых мартышек) либо отбирая естественные авирулентные штаммы. В настоящее время возможен путь создания живых вакцин путем генной инженерии на уровне хромосом с использованием рестриктаз. Полученные штаммы будут обладать свойствами обеих возбудителей, хромосомы которых были взяты для синтеза. Анализируя свойства живых вакцин следует выделить, как положительные так и их отрицательные качества.
Положительные стороны: по механизму действия на организм напоминают "дикий" штамм, может приживляться в организме и длительно сохранять иммунитет (для коревой вакцины вакцинация в 12 мес. и ревакцинация в 6 лет), вытесняя "дикий" штамм. Используются небольшие дозы для вакцинации (обычно однократная) и поэтому вакцинацию легко проводить организационно. Последнее позволяет рекомендовать данный тип вакцин для дальнейшего использования.
Отрицательные стороны: живая вакцина корпускулярная - содержит 99% балласта и поэтому обычно достаточно реактогенная, кроме того, она способна вызывать мутации клеток организма (хромосомные аберрации), что особенно опасно в отношении половых клеток. Живые вакцины содержат вирусы-загрязнители (контаминанты), особенно это опасно в отношении обезьяннего СПИДа и онковирусов. К сожалению, живые вакцины трудно дозируются и поддаются биоконтролю, легко чувствительны к действию высоких температур и требуют неукоснительного соблюдения холодовой цепи. Хотя живые вакцины требуют специальных условий хранения, они продуцируют достаточно эффективный клеточный и гуморальный иммунитет и обычно требуют лишь одно бустерное введение. Большинство живых вакцин вводится парентерально (за исключением полиомиелитной вакцины).
На фоне преимуществ живых вакцин имеется и одно предостережение, а именно: возможность реверсии вирулентных форм, что может стать причиной заболевания вакцинируемого. По этой причине живые вакцины должны быть тщательно протестированы. Пациенты с иммунодефицитами (получающие иммуносупрессивную терапию, при СПИДе и опухолях) не должны получать такие вакцины.
Примером живых вакцин могут служить вакцины для профилактики краснухи (Рудивакс), кори (Рувакс), полиомиелита (Полио Сэбин Веро), туберкулеза, паротита (Имовакс Орейон). Живые вакцины выпускаются в лиофилизированном виде (кроме полиомиелитной).
Ассоциированные вакцины
Вакцины различных типов, содержащие несколько компонентов (АКДС).
Корпускулярные вакцины
Представляют собой бактерии или вирусы, инактивированные химическим (формалин, спирт, фенол) или физическим (тепло, ультрафиолетовое облучение) воздействием. Примерами корпускулярных вакцин являются: коклюшная (как компонент АКДС и Тетракок), антирабическая, лептоспирозная, гриппозные цельновирионные, вакцины против энцефалита, против гепатита А (Аваксим), инактивированная полиовакцина (Имовакс Полио, или как компонент вакцины Тетракок).
Сегодня перед каждым родителем встает важнейший вопрос вакцинирования ребенка. Да и самим взрослым периодически необходимо ставить прививки . Многие сторонники «естественной медицины» уверяют, что вакцинация — это опасное и вредное мероприятие, которое служит ослаблению иммунитета и направлено на финансирование медицинских экспериментов. Но давайте отложим все «теории заговора» и подойдем к вопросу о вакцинировании честно и беспристрастно.
Цель вакцинации
Прежде чем рассуждать о типах вакцин, следует разобраться в том, что такое вакцина вообще.
Вакцина — это вещество, которое позволяет организму приобрести временную или постоянную невосприимчивость к тому или иному виду вирусов. Механизм работы вакцины довольно прост и понятен — вещество, содержащее в себе мизерную долю микроорганизмов или продуктов их жизнедеятельности, вводится в организм человека. Организм «знакомится» с таким веществом и при встрече с настоящим вирусом проявляет стойкий иммунитет.
Вакцинация помогает защититься от тяжелых вирусных заболеваний: , оспы , полиомиелита, паротита. Организм вырабатывает иммунитет к этим заболеваниям и становится устойчив к вирусам.
Опасности вакцинации
Следует сказать пару слов об опасностях вакцинирования. Действительно, некоторые люди, особенно дети, могут проявить аллергические реакции после введения вакцины. Обычно они выражаются в раздражении кожи, зуде, покраснении. Однако следует отметить, что:
- крайне малый процент детей (менее 1%) проявляет аллергию;
- состав вакцин каждый год улучшается и становится все более гипоаллергенным (то есть безопасным для людей с аллергией);
- ваш ведущий педиатр знает обо всех аллергенах вашего ребенка и может предположить, на какие вакцины может быть аллергия;
- аллергическая реакция на вакцину — ничто по сравнению с настоящим заболеванием.
Состав вакцины
Для выработки иммунитета ученые используют следующие типы раздражителей:
- живые микроорганизмы;
- ослабленные или убитые микроорганизмы;
- химически синтезированные антигены;
- продукты жизнедеятельности микроорганизмов.
Живые и неживые вакцины
Живыми называют вакцины, в составе которых есть настоящие естественные микроорганизмы. Неживыми — все остальные. Многие родители предполагают, что живые вакцины более эффективны и безопасны для ребенка, однако на самом деле это правда лишь отчасти. Давайте рассмотрим различия между живыми и неживыми вакцинами.
- Безопасность для организма. И живые, и неживые вакцины безвредны и безопасны в одинаковой степени. Нет никаких статистических или научных данных о том, что один вид вакцин чаще вызывает аллергическую реакцию. Не следует бояться синтезированных антигенов. Однако живые вакцины не вводят людям с заболеваниями, вызывающими проблемы с иммунитетом. Это лейкемия, ВИЧ, а также болезни, которые лечатся препаратами с подавлением иммунной системы. Это связано с тем, что живой штамм при сниженном иммунитете носителя может начать размножаться и привести к настоящему заболеванию.
- Эффективность. Живые вакцины позволяют добиться долгосрочного (зачастую даже пожизненного) иммунитета к заболеванию, в то время как неживые необходимо обновлять раз в несколько лет. Однако неживые вакцины способны добиться появления стойкого иммунитета независимо от наличия и количества циркулирующих антител в крови пациента.
- Скорость воздействия. После введения живой вакцины результат проявляется практически мгновенно. Неживая вакцина требует нескольких (обычно двух-трех) вакцинаций, чтобы подействовать на организм.
